Zawartość
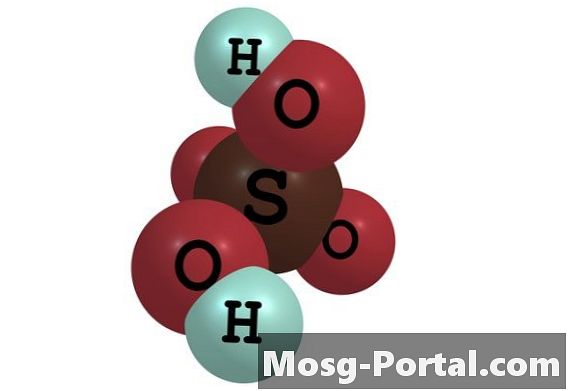
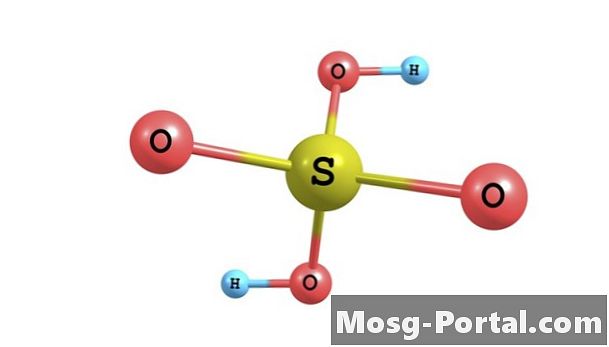
Kwas siarkowy jest silnym kwasem nieorganicznym powszechnie stosowanym w przemysłowej produkcji chemikaliów, w pracach badawczych i w warunkach laboratoryjnych. Ma wzór cząsteczkowy H2SO4. Jest rozpuszczalny w wodzie we wszystkich stężeniach, tworząc roztwór kwasu siarkowego. W roztworze mol kwasu siarkowego rozdziela się na mol ujemnie naładowanych jonów siarczanowych lub SO4 (2-) i 2 mole dodatnio naładowanych jonów hydroniowych lub H3O +. Stężenie tych jonów wyraża się w molowości, która jest zdefiniowana jako liczba moli jonów na litr roztworu. Ich stężenie zależy od początkowego stężenia kwasu siarkowego.